Calor
El sol suele dar una sensación de calor.
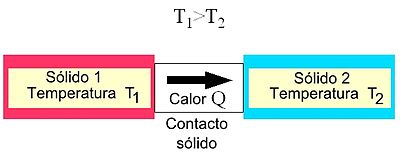
Esquema de la transferencia de calor por conducción.
La energía calórica o térmica puede ser transferida por diferentes mecanismos de transferencia, estos son la radiación, la conducción y la convección, aunque en la mayoría de los procesos reales todos se encuentran presentes en mayor o menor grado. Cabe resaltar que los cuerpos no tienen calor, sino energía térmica. La energía existe en varias formas. En este caso nos enfocamos en el calor, que es el proceso mediante el cual la energía se puede transferir de un sistema a otro como resultado de la diferencia de temperatura.
Calor específico
El calor específico es la energía necesaria para elevar 1*C la temperatura de un gramo de materia. El concepto de capacidad calorifica es análogo al anterior pero para una masa de un mol de sustancia (en este caso es necesario conocer la estructura quimica de la misma).
El calor específico es un parámetro que depende del material y relaciona el calor que se proporciona a una masa determinada de una sustancia con el incremento de temperatura:
donde:
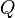 es el calor aportado al sistema.
es el calor aportado al sistema.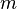 es la masa del sistema.
es la masa del sistema. es el calor específico del sistema.
es el calor específico del sistema.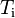 y
y 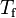 son las temperaturas inicial y final del sistema respectivamente.
son las temperaturas inicial y final del sistema respectivamente. es el diferencial de temperatura.
es el diferencial de temperatura.
El calor específico de un material depende de su temperatura; no obstante, en muchos procesos termodinámicos su variación es tan pequeña que puede considerarse que el calor específico es constante. Asimismo, también se diferencia del proceso que se lleve a cabo, distinguiéndose especialmente el "calor específico a presión constante" (en un proceso isobarico) y "calor específico a volumen constante (en un proceso isocorico).
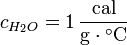

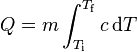
No hay comentarios:
Publicar un comentario