Proceso termodinámico
En física, se denomina proceso termodinámico a la evolución de determinadas magnitudes (o propiedades) propiamente termodinámicas relativas a un determinado sistema termodinámico. Desde el punto de vista de la termodinámica, estas transformaciones deben transcurrir desde un estado de equilibrio inicial a otro final; es decir, que las magnitudes que sufren una variación al pasar de un estado a otro deben estar perfectamente definidas en dichos estados inicial y final. De esta forma los procesos termodinámicos pueden ser interpretados como el resultado de la interacción de un sistema con otro tras ser eliminada alguna ligadura entre ellos, de forma que finalmente los sistemas se encuentren en equilibrio (mecánico, térmico y/o material) entre sí.
De una manera menos abstracta, un proceso termodinámico puede ser visto como los cambios de un sistema, desde unas condiciones iniciales hasta otras condiciones finales, debido a la desestabilización del sistema.
Tipos de procesos termodinámicos
Procesos Iso
Son los procesos cuyas magnitudes permanecen "constantes", es decir que el sistema cambia manteniendo cierta proporcionalidad en su transformación. Se les asigna el prefijoiso-.
Ejemplo:
- Isotérmico: proceso a temperatura constante
- Isobárico: proceso a presión constante
- Isométrico o isocórico: proceso a volumen constante
- Isoentálpico: proceso a entalpía constante
- Isoentrópico: proceso a entropía constante
Procesos politrópicos
Los procesos politrópicos son aquellos procesos termodinámicos para gases ideales que cumplen con la ecuación:  donde
donde 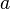 es un número dado. Para el caso de procesos adiabáticos,
es un número dado. Para el caso de procesos adiabáticos, 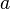 es igual a
es igual a 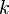 , el cual es un valor específico para cada sustancia. Este valor se puede encontrar en tablas para dicho caso.
, el cual es un valor específico para cada sustancia. Este valor se puede encontrar en tablas para dicho caso.
 donde
donde 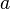 es un número dado. Para el caso de procesos adiabáticos,
es un número dado. Para el caso de procesos adiabáticos, 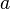 es igual a
es igual a 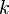 , el cual es un valor específico para cada sustancia. Este valor se puede encontrar en tablas para dicho caso.
, el cual es un valor específico para cada sustancia. Este valor se puede encontrar en tablas para dicho caso.
No hay comentarios:
Publicar un comentario